RESUMEN
La etiqueta para la tos y la higiene respiratoria son formas de control de la fuente de emisión cuyo uso se alienta para evitar la propagación de infecciones respiratorias. El uso de mascarillas quirúrgicas como medio de control de la fuente en términos de reducción de la exposición de terceros no se ha investigado. En este estudio diseñamos un modelo in vitro utilizando varias mascarillas faciales con el fin de evaluar su aporte a la reducción de la exposición cuando son utilizadas en la fuente infecciosa (Fuente) en comparación con la reducción proporcionada por las mascarillas usadas para la protección primaria (Receptor), así como los factores que contribuyen a cada una. En una cámara con diversos flujos de aire se exhalaron aerosoles radiomarcados desde una cabeza de maniquí de cara blanda ventilada, utilizando respiración periódica y tos (Fuente). En otro maniquí, al que se le colocó un filtro, se cuantificó la exposición del Receptor. Se probaron una mascarilla quirúrgica de ajuste natural, una mascarilla quirúrgica de ajuste seguro (SecureFit) y una mascarilla respiratoria autofiltrante de clase N95 (comúnmente conocida como "mascarilla autofiltrante N95") con y sin sello de vaselina. Con la tos, el control de la fuente (mascarilla quirúrgica/autofiltrante colocada en la Fuente) fue estadísticamente superior a la protección brindada por la mascarilla quirúrgica/mascarilla autofiltrante sin sellar en el Receptor (protección del Receptor) en todos los entornos. Para igualar el control de la fuente durante la tos, la mascarilla autofiltrante N95 debe estar sellada con vaselina. Durante la respiración periódica, el control de la fuente fue comparable o superior a la protección brindada por la mascarilla quirúrgica/autofiltrante en el Receptor. El control de la fuente mediante mascarillas quirúrgicas puede ser una importante defensa adicional contra la propagación de infecciones respiratorias. El ajuste de la mascarilla quirúrgica/autofiltrante combinado con los patrones de flujo de aire en un entorno determinado contribuye de manera significativa a la eficacia del control de la fuente. Los futuros ensayos clínicos deberían incluir un brazo de control de la fuente con mascarilla quirúrgica a fin de evaluar el aporte realizado por el control de la fuente a la protección general contra infecciones de transmisión aérea.
Introducción
En la última década, la aparición de nuevos virus de transmisión aérea y el resurgimiento de la tuberculosis han planteado importantes amenazas para la salud pública. Por el momento no se ha definido con claridad cuál es el medio de protección más adecuado para el personal sanitario contra estas amenazas.[Citation1,Citation2] Algunos estudios han sugerido el uso de mascarillas quirúrgicas por el personal de la salud como barrera de protección durante la inhalación.[Citation3,Citation4] Sin embargo, las mascarillas quirúrgicas no han sido probadas ni certificadas para su uso como dispositivos de protección respiratoria. El Código de Regulaciones Federales (Code of Federal Regulations, CFR) de la Administración de Alimentos y Medicamentos (Food and Drug Administration, FDA) de los Estados Unidos, Título 21 CFR 878.4040, las clasifica de manera general entre los dispositivos médicos destinados a proteger a los pacientes y las personas en contacto con ellos de la transferencia de microorganismos, fluidos corporales y materiales particulados. Las mascarillas autofiltrantes, en cambio, se consideran dispositivos de protección durante la inhalación.[Citation5–7] A menudo, las recomendaciones regulatorias se basan en evaluaciones in vitro de la eficacia de la filtración. [Citation8–10]
No obstante, los estudios in vivo clínicamente pertinentes son limitados y pueden no reflejar los datos obtenidos in vitro.[Citation11] Por ejemplo, los estudios realizados durante los brotes de SARS y H1N1 no lograron demostrar la existencia de diferencias significativas en las tasas de infección del personal sanitario que usaba mascarillas quirúrgicas/autofiltrantes.[Citation4, Citation12, Citation13] Además, los estudios in vitro han demostrado que las mascarillas autofiltrantes N95/quirúrgicas pueden tener un desempeño inferior al esperado ante la presencia de virus de partículas de menor tamaño, como la gripe [Citation8, Citation14] Reponen et al. informaron que, por su tamaño físico, el coronavirus SARS y el virus de la gripe tienen alta penetración, tanto a través de las mascarillas quirúrgicas como de las N95.[Citation14] Ambos tipos de mascarillas son consideradas como Equipo de Protección Personal (EPP) debido a los distintos beneficios de protección que ofrecen. El Instituto Nacional de Seguridad y Salud Ocupacional (Institute for Occupational Safety and Health, NIOSH) y la Administración de Salud y Seguridad Ocupacional (Occupational Health and Safety Administration, OSHA) caracterizan al EPP como "la última línea de defensa", alentando la realización de controles administrativos y de ingeniería para mitigar la exposición al entorno. Nuestro estudio evalúa la eficacia de las mascarillas quirúrgicas para proporcionar protección secundaria al personal sanitario y a otros en relación con las mascarillas quirúrgicas y autofiltrantes utilizadas para protección personal.
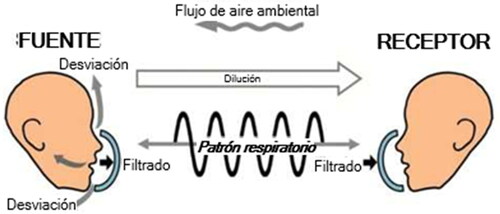
Recientemente, Díaz y Smaldone modelaron los efectos provocados por la transmisión de aerosoles relacionados con las mascarillas entre individuos. Si bien su modelo incluía los efectos de la filtración, también consideraba la interacción de otros factores importantes.[Citation15] Como se muestra en la , incluyeron el flujo de aire ambiental en la habitación, la protección brindada por la mascarilla, los efectos de la desviación (por ejemplo, la fuga del sellado facial) y la filtración, con mascarillas colocadas en la Fuente infecciosa o en el Receptor. El aporte de la desviación (fuga hacia el exterior en torno al perímetro del sellado facial) se determinó comparando las mascarillas N95 con y sin sello de vaselina. Encontraron que, a menudo, el control de la fuente (mascarilla en la Fuente) era 3–300 veces más eficaz que una mascarilla colocada en el Receptor. Los factores interactivos de ese estudio se limitaron a la respiración periódica, los efectos de presión negativa en la habitación y el uso de un maniquí de plástico duro. Para estudiar con mayor profundidad el modelo de Díaz y Smaldone, ampliamos el modelo de referencia in vitro utilizando un nuevo maniquí realista blando, con el objetivo de probar tres ambientes de flujo de aire durante la respiración periódica y la tos.
Figura 1. Modelo de maniquí fuente, maniquí receptor e interacción con el entorno. Modelo de maniquí fuente, maniquí receptor e interacción con el entorno. Los parámetros se pueden establecer o medir. La dilución es un efecto del entorno en la concentración de los aerosols producidos. La filtración (eficiencia de captura) es una función de la mascarilla utilizada y tiene lugar tanto en la fuente como en el receptor. Las partículas que no son capturadas pueden ser desviadas (fuga hacia el exterior alrededor del perímetro del sellado facial) por la mascarilla en la fuente y llevadas lejos del receptor por el flujo ambiental. Los patrones de respiración simulan a los adultos con respiración periódica o tos.
Métodos
Cámara de exposición
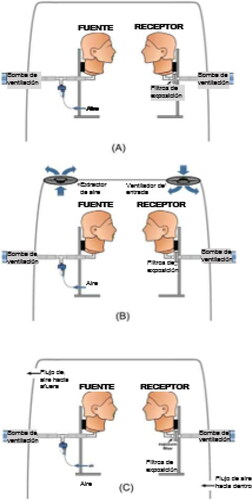
Para cuantificar la exposición se modificó el diseño de la cámara de Díaz y Smaldone. Construimos un modelo a escala de la habitación de un solo paciente en nuestro hospital (204 piesCitation3, 6–25 pies de largo x 5.25 pies de ancho x 6.25 pies de alto). Se eligieron tres regímenes de flujo diferentes (): () sin flujo de aire ambiental (0 intercambio de aire por hora), todo el movimiento de aire en la cámara era secundario a la tos o la respiración de la Fuente y el Receptor; () modelo de una habitación típica de hospital equipada con un ventilador de techo de entrada y salida (6 intercambios de aire por hora);[Citation16, Citation17] y (), modelo de una habitación típica de hospital con presión negativa, la cámara estaba equipada con un extractor ubicado detrás de la cabeza del maniquí Fuente cuyo flujo unidireccional estaba definido desde la entrada hasta el respiradero detrás de la Fuente (12 intercambios de aire por hora).[Citation18] La dirección apropiada del flujo en la sala de presión negativa fue comprobada usando pruebas de humo. Se ajustó el flujo de la cámara en pies3/min (FCM) regulando los ventiladores con un balonómetro (modelo 6200D; Alnor, Huntington Beach, CA). El FCM se convirtió en intercambios de aire por hora (IAH) usando la fórmula: IAH = (FCM x 60 min)/(volumen de la habitación en pies cúbicos). La humedad relativa y la temperatura de la cámara se midieron diariamente y oscilaron entre 33–58% y 21.0–22.8°C, respectivamente. Ajustamos el flujo de aire en la cámara usando un factor de escala. Este factor se definió como la relación entre el volumen de una habitación de hospital y el volumen de nuestra cámara, por ejemplo, 8.41, para crear ventilación tanto en 6 IAH (171 FCM) como en 12 IAH (343 FCM). Dicho ajuste fue necesario porque nuestros parámetros de ventilación (por ejemplo, los volúmenes de respiración periódica y de tos) correspondían a individuos normales, pero el volumen de la cámara de pruebas era menor que el de una habitación estándar.[Citation19, Citation20] A medida que el volumen de la cámara de pruebas disminuye en relación con el volumen de la respiración periódica, el aporte este último por respiración aumenta proporcionalmente, incrementando la concentración de partículas por respiración con la disminución del volumen de la habitación. Para corregir esta situación, el flujo de intercambio de aire debe aumentarse de manera proporcional.[Citation16]
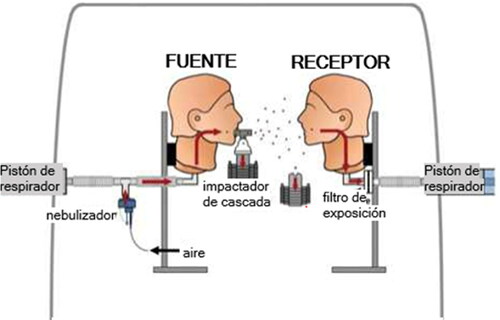
Figura 2. Cámara sin flujo, 0 intercambios de aire por hora (IAH). Representación esquemática que ilustra una cámara que contiene las cabezas de maniquíes ventiladas a 3 pies de distancia. La cabeza de la Fuente estaba conectada a un nebulizador y exhaló aerosoles radioactivos. Se colocó un filtro en la cabeza del Receptor para capturar y cuantificar los aerosoles radioactivos inhalados (exposición) (A). Cámara de habitación de hospital, con 6 IAH. Representación esquemática que ilustra una cámara que contiene las cabezas de maniquíes ventiladas a 3 pies de distancia. La cabeza de la Fuente estaba conectada a un nebulizador y exhaló aerosoles radioactivos. Se colocó un filtro en la cabeza del Receptor para capturar y cuantificar los aerosoles radioactivos inhalados (exposición) (B). Cámara de habitación con presión negativa, con 12 IAH. Representación esquemática que ilustra una cámara que contiene las cabezas de maniquíes ventiladas a 3 pies de distancia. La cabeza de la Fuente estaba conectada a un nebulizador y exhaló aerosoles radioactivos. Se colocó un filtro en la cabeza del Receptor para capturar y cuantificar los aerosoles radioactivos inhalados (exposición) (C).
Dentro de la cámara se colocaron dos maniquíes de resucitación cardiopulmonar (CPR) Resusci Anne (No. 310200; Laerdal Medical) a poco más de tres pies de distancia, inmediatamente fuera del área definida como de contacto cercano (<3 pies) por los Centros para el Control y Prevención de Enfermedades (CDC). A esta distancia el personal sanitario está expuesto a un mayor riesgo de infección por aerosoles cuando se producen las actividades que los generan, como la tos.Citation3 Esto se imitó en dos individuos colocados en una habitación. Cada maniquí estaba conectado a una bomba de ventilación de Harvard (Aparato Harvard SN No. A52587; Millis, MA). Las cabezas de los maniquíes Resusci Anne CPR tienen tamaño real (basado en el molde de un rostro femenino real), poseen caras blandas y deformables y "textura de piel". Recientemente se publicó un estudio detallado que prueba el ajuste de la mascarilla en este maniquí.[Citation21]
Luego, durante la respiración periódica o la tos, se liberaron aerosoles desde la Fuente. En un maniquí ventilado idéntico, el Receptor, se colocó un filtro diseñado para capturar todas las partículas inhaladas, con el fin de cuantificar la exposición del trabajador de la salud.
Patrones de respiración y aerosoles de la prueba
Se analizaron la respiración periódica y la tos en la Fuente. En todos los experimentos la bomba del Receptor fue configurada para la respiración periódica (volumen de marea de 500 mL, frecuencia respiratoria de 15 respiraciones/min, y ciclo de trabajo del 50%).[Citation19, Citation20] La bomba de la Fuente fue configurada para el mismo patrón de respiración periódica o, en una serie separada de experimentos, para la tos. Mediante una serie de respiraciones de 1.5 litros generadas por la bomba se produjo una tos simulada, con un flujo máximo de 5.2 L/s. Como se muestra en la , el nebulizador se conectó en serie con el maniquí Fuente. Para cada tos se activaba primero el nebulizador, llenando el tubo inspiratorio con aerosol (5s.), y luego se activaba la bomba de Harvard y se expulsaba rápidamente todo el volumen (1s.). Esta maniobra se repitió 20 veces durante un periodo de recolección de ocho minutos. En el Receptor se mantuvo un patrón de respiración periódica durante la tos. La cámara fue lavada con aire limpio en los intervalos entre los experimentos para evitar la contaminación cruzada.
Los nebulizadores se eligieron con base en las características del aerosol reportado en humanos durante la respiración periódica y la tos.[Citation22, Citation23] Los aerosoles de respiración periódica fueron creados por un nebulizador AeroTech II (Biodex, Shirley, NY) alimentado por un tanque de aire a 10 L por minuto. Situado en línea con la Fuente (), el nebulizador se llenó con 3 mL de solución salina normal al 0.9%, etiquetada con tecnecio-99m, y funcionó durante ocho minutos. El flujo del tanque de aire se superpuso al patrón de ventilación durante la respiración periódica. Los aerosoles de la tos se generaron utilizando tres nebulizadores de chorro Salter 8900, usados en rotación (Salter Labs, Arvin, CA), conectados a un compresor Salter Aire.
Los aerosoles húmedos radiomarcados simulaban partículas infecciosas liberadas durante la respiración periódica y la tos. Durante el periodo de ocho minutos, la salida del nebulizador fue constante. En experimentos separados se midieron las distribuciones de los diámetros aerodinámicos de las partículas en las cabezas de los maniquíes de la Fuente y el Receptor empleando la impactación en cascada (impactador Marple de 8 etapas; Thermo Fischer Scientific, Waltham, MA; flujo de 2 L por minuto) (). Los aerosoles cercanos al Receptor fueron medidos sin la presencia de mascarillas colocadas en la Fuente o el Receptor. Las distribuciones se trazaron en un papel de probabilidad logarítmica. Los datos fueron reportados como DMMA (diámetro de masa media aerodinámico), una distribución logarítmica normal acumulativa de los diámetros aerodinámicos, el percentil 84.1 dividido entre el percentil 15.9 DEG (desviación estándar geométrica) definida.
Exposición y protección de la mascarilla
La exposición del Receptor al aerosol se cuantificó colocando un filtro (modelo No. 041B0522; Pari, Starnberg, Alemania) en el maniquí Receptor; este capturó todas las partículas inhaladas (). Todos los gases y las partículas inhaladas pasaron de la boca al filtro a través de tubos sellados. No hubo ventilación que pasara por la nariz.
La primera serie de experimentos se realizó sin colocar mascarillas en ninguno de los maniquíes. Esto definió la "Exposición Máxima" (MaxEx), reportada como el porcentaje de partículas nebulizadas capturadas (es decir, inhaladas) por el Receptor.
Luego, probamos tres tipos de mascarillas: una mascarilla autofiltrante de clase N95 (modelo No. 1860S tamaño pequeño; 3M, St. Paul, MN), una mascarilla quirúrgica con bucle de oreja de ajuste natural (modelo No. GCFCXS; Crosstex International Inc, Hauppauge, NY) y una mascarilla quirúrgica con ajuste SecureFit Ultra (modelo No. GCFCXUSF; Crosstex International Inc, Hauppauge, NY). Tanto las mascarillas quirúrgicas de ajuste natural como las SecureFit poseían idénticos materiales de filtración (BFE > 99.9% a 3 micrones, PFE = 99.8% a 0.1 micrones, Delta P < 5.0 H2O/cm2), los cuales cumplen con las normas de nivel 3 de la Sociedad Americana de Pruebas y Materiales (American Society for Testing and Materials, ASTM). Se evaluaron varias combinaciones de mascarillas: sin mascarilla (exposición máxima), la mascarilla quirúrgica (SMnat), la mascarilla quirúrgica ajustada SecureFit Ultra (SF), la mascarilla autofiltrante N95 (N95) y la mascarilla autofiltrante N95 con sello de vaselina (N95vas). El sello se creó con una costura de vaselina colocada alrededor del perímetro de la mascarilla autofiltrante, ya sea en la fuente o en el receptor, y la fuga se probó con jabón líquido. Las mascarillas quirúrgicas nunca fueron selladas a la cara. Para permitir la comparación entre el control de la Fuente y los efectos de protección personal en trabajadores sanitarios, se probaron mascarillas quirúrgicas y autofiltrantes N95 en el Receptor, esta última con y sin sello de vaselina.
La mascarilla quirúrgica/autofiltrante N95 colocada únicamente en la Fuente sirvió para evaluar los efectos combinados de dos variables: la eficiencia de captura (definida como el aerosol capturado por la mascarilla) y la desviación (definida como la fuga hacia afuera que tiene lugar alrededor del perímetro del sellado facial de la mascarilla), . La filtración pura de los aerosoles fuente se midió tras sellar la mascarilla autofiltrante N95 a la cara con vaselina, eliminando toda posible fuga.
Medidas
La exposición al aerosol se cuantificó midiendo la radioactividad capturada por el filtro del maniquí Receptor. Estos valores se normalizaron para la cantidad de radioactividad dejada por el nebulizador en un recorrido dado, corregido por las pérdidas del tubo desde el nebulizador hasta los "labios" del maniquí Fuente (porcentaje de Actividad Exhalada). Esta radioactividad representa el aerosol que llega a la mascarilla colocada en la Fuente. La filtración de las mascarillas colocadas en la Fuente se midió determinando la radioactividad en estas como un porcentaje de la Actividad Exhalada. Las mediciones se hicieron con un calibrador de dosis (0.01 micro Curies (μCi)-9999 mCi; Biodex, Shirley, NY), un medidor de tasa calibrado (<10 μCi; Ludlum Measurements Inc, Sweetwater, TX), o una microcélula calibrada (10 μCi–10 mCi; Kemble Instruments, Hamden, CT). La eficiencia de captura es la cantidad de radioactividad exhalada por la Fuente capturada en el filtro colocado en esta.
Estadísticas
Los datos de la exposición y la eficiencia de captura de la mascarilla se expresaron como porcentaje de partículas nebulizadas (media con los correspondientes intervalos de confianza [IC] de 95% por ambos lados). Los datos del grupo se compararon utilizando el análisis de varianza de Kruskal-Wallis; un valor p <0.05 definió la significación estadística. Los cálculos se hicieron empleando el GraphPad Prism v6.0 para Mac OS X (GraphPad Software, San Diego, CA). Para efectos de comparación, calculamos un factor de protección del Receptor (FPR), definido como la relación entre la MaxEx y la exposición real.
Resultados
Distribución de las partículas de aerosol
Las distribuciones de partículas, DMMA y DEG, se resumen en la . Se presentan las distribuciones de partículas para las tres habitaciones, tanto en la Fuente como en el Receptor. Durante la tos, se constató que en la Fuente, en las tres habitaciones, las distribuciones contenían partículas más grandes que en el caso de la respiración periódica. Cuando las partículas emitidas durante la tos alcanzaron al Receptor, los diámetros disminuyeron significativamente, debido a la contracción o el asentamiento. Durante la respiración periódica se observaron efectos de reducción menores e insignificantes.
Tabla 1. Distribuciones de partículas descritas por el diámetro de masa media aerodinámico (DMMA) y la desviación estándar geométrica (DEG) para la respiración periódica y la tos. El DMMA se expresa en μm.
Exposición y protección de la mascarilla: respiración periódica
Los datos de exposición y MaxEx se muestran en la , con el correspondiente FPR para cada configuración de mascarilla que aparece en la . Los datos de la cifra se reportan como porcentaje de partículas nebulizadas. MaxEx indica el efecto de la dilución debida al flujo ambiental y se le asigna un FPR de 1, que representa la no protección. Para derivar el FPR, se utilizaron los valores medios de los datos de exposición. En las habitaciones sin flujo, de hospitales y de presión negativa, la MaxEx promedió en 1.146% (95% CI: 1.037–1.255%), 0.617% (95% CI: 0.577–0.657%) y 0.0167% (95% CI: 0.0152–0.0182%), respectivamente.
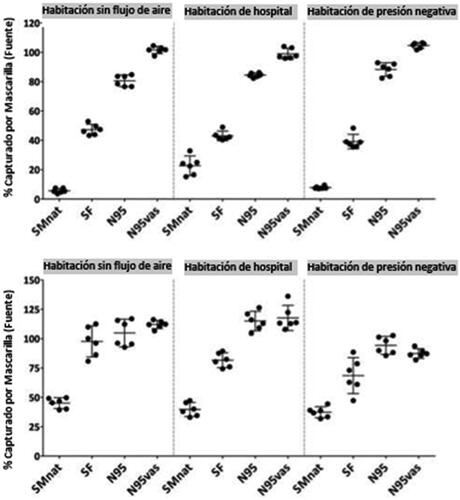
Figura 4. Los datos de exposición para la respiración periódica, expresados como porcentaje del aerosol exhalado con un IC de 95% de dos lados, trazados para diferentes mascarillas en la Fuente o el Receptor. Un asterisco (*) denota el significado de un valor-p <0.05 usando la prueba de Kruskal-Wallis. F = Fuente, R = Receptor, MaxEx = Exposición Máxima, SMnat = Mascarilla quirúrgica de ajuste natural, SF = Mascarilla quirúrgica de ajuste SecureFit Ultra, N95 = Mascarilla autofiltrante 3M N95, N95vas = Mascarilla autofiltrante 3M N95 con sello de vaselina.
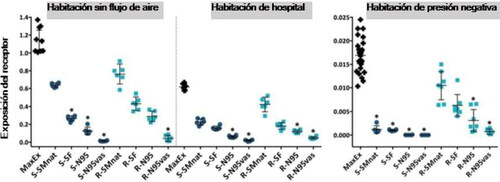
Tabla 2. Factores de protección respiratoria (FPR) para la respiración periódica y la tos. Un asterisco (*) denota el significado de un valor-p < 0.05 usando el análisis unidireccional de varianza de Kruskal-Wallis
El efecto de cada intervención de la mascarilla en la reducción de la exposición es ilustrado de mejor manera por el cambio en el FPR ().
Se observaron importantes diferencias entre las habitaciones. Para la habitación sin flujo de aire, la mascarilla colocada en la Fuente fue estadísticamente superior en los casos de la mascarilla quirúrgica ajustada SecureFit Ultra y la mascarilla autofiltrante N95 con y sin sello de vaselina. La única mascarilla que proporcionó resultados significativamente diferentes en el Receptor fue la N95 con sello de vaselina. Las diferencias entre los tipos de mascarillas fueron significativas, lo que indica que el principal mecanismo de protección fue la filtración. En la habitación de hospital se observaron hallazgos similares: con una mejor filtración la exposición se redujo al utilizar una mascarilla N95 con y sin sello de vaselina en la Fuente o el Receptor. La revisión de los datos del FPR de la habitación de hospital indica que, en general, la exposición fue menor (mayor FPR) cuando la mascarilla autofiltrante estaba en la Fuente. Sin embargo, esto no fue estadísticamente significativo. En la sala de presión negativa, la aplicación de una mascarilla quirúrgica o una mascarilla autofiltrante en la Fuente dio lugar a reducciones estadísticamente significativas de la exposición, mientras que en el Receptor solo la mascarilla N95 con o sin sello de vaselina proporcionó una protección similar. Mientras se registraron diferencias significativas entre algunas mascarillas (por ejemplo, el efecto de eficiencia de captura, SMnat vs. N95 vs. N95vas), en la habitación de presión negativa las principales diferencias en la exposición respondieron a la fuga de partículas hacia afuera alrededor del perímetro del sellado facial (desviación) en la Fuente. En este ambiente, las partículas desviadas son rápidamente arrastradas por el flujo de aire. Esta observación resulta más evidente cuando se compara el FPR de la Fuente y el Receptor. Cada mascarilla de la Fuente redujo notablemente la exposición del Receptor, incluso cuando la mascarilla poseía baja eficiencia de captura. En este caso, la desviación fue el mecanismo más importante para reducir la exposición del receptor.
Exposición y protección de la mascarilla: tos
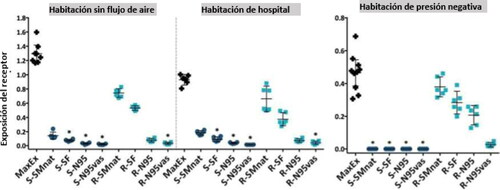
Los datos sobre la tos se muestran en y en el panel inferior de la . En comparación con la respiración periódica, existen grandes diferencias en la magnitud y en los mecanismos de exposición. En general, en todas las habitaciones la mascarilla de la Fuente fue superior a la del Receptor. Los resultados fueron relativamente insensibles para capturar la eficiencia, es decir, una mascarilla N95 colocada en el Receptor y una mascarilla quirúrgica de ajuste natural colocada en la Fuente mostraron la misma eficacia (sala sin flujo y sala de hospital) o esta última fue más eficaz (sala de presión negativa). En comparación con la respiración periódica, la reducción de la exposición a la tos es probablemente una función de la impactación de partículas más grandes en cualquier mascarilla/mascarilla autofiltrante colocada en la Fuente.
Figura 5. Los datos de exposición para la tos, expresados como un porcentaje del aerosol exhalado con un IC de 95% de dos caras, trazados para diferentes mascarillas en la Fuente o el Receptor. Un asterisco (*) denota el significado de un valor-p <0.05 usando la prueba de Kruskal-Wallis. F = Fuente, R = Receptor, MaxEx = Exposición Máxima, SMnat = Mascarilla quirúrgica de ajuste natural, SF = Mascarilla quirúrgica de ajuste SecureFit Ultra, N95 = Mascarilla autofiltrante 3M N95, N95vas = Mascarilla autofiltrante 3M N95 con sello de vaselina.
Filtración en la fuente
En la se muestra la eficiencia de captura de la mascarilla (captura de las partículas que salen de la Fuente) para las diversas piezas faciales. En el caso de la respiración periódica (panel superior), se observó un patrón típico de eficiencia de captura: la mascarilla quirúrgica de ajuste natural capturó las partículas de manera deficiente, debido a su fuga hacia afuera alrededor del perímetro del sellado facial (∼5–20%). Al aplicar un mejor ajuste y reducir las fugas de la mascarilla usando los filtros de la mascarilla quirúrgica ∼50%, el N95 ∼ 80–90% y un N95 sellado ∼100%, se observó un patrón diferente durante la tos ( - panel inferior). La eficiencia de captura de partículas se incrementó tanto para las mascarillas quirúrgicas como para las autofiltrantes, de manera que, con el aumento de ajuste proporcionado por la SM, tanto la mascarilla quirúrgica SM como la N95 capturan ∼100% del aerosol exhalado.
Discusión
Nuestros datos cuantifican la sinergia potencial entre el control de la fuente y las mascarillas y la protección personal con dispositivos de protección respiratoria. Combinado con los controles ambientales, el control de la fuente puede ser más eficaz que la protección personal por sí sola.
El presente estudio se centró en el uso de mascarillas quirúrgicas y autofiltrantes como medio para reducir la contaminación ambiental mediante una barrera de protección colocada en la fuente y no sugiere ni apoya el uso de mascarillas quirúrgicas como medio de protección respiratoria. Tampoco aborda las numerosas variables asociadas a dicha protección, como la dosis infecciosa y los modos de transmisión, que pueden variar significativamente con cada amenaza infecciosa. Más bien, utilizamos medidas de protección respiratoria in vitro como el FPR, como medio para correlacionar la reducción de la exposición con el control de la fuente, lo que se logra usando diferentes mascarillas quirúrgicas o autofiltrantes en el receptor. Nuestros hallazgos apoyan el uso de mascarillas como medio potencialmente fiable y consistente de control de infecciones, similar a otros controles ambientales, por ejemplo, la etiqueta en la respiración, el lavado de manos, la separación física y los controles de ingeniería, como las salas de aislamiento de presión negativa. Aunque aquí se utilizan los términos "pacientes" y "personal sanitario" para identificar las "Fuentes" y "Receptores" más obvios en un ambiente hospitalario, probablemente nuestros datos puedan aplicarse a cualquier combinación de posibles "Fuentes" y "Receptores", por ejemplo, visitas a hospitales, personal sanitario que no ha recibido la vacuna contra la gripe o pacientes dentro de entornos de atención sanitaria, como salas de emergencia y salas de espera de consultorios médicos.
Si bien se necesitan estudios clínicos que confirmen nuestras observaciones, el análisis de los mecanismos de exposición ilustrados en la , combinado con nuestros datos cuantitativos, sugiere el control de la fuente como un enfoque para reducir la exposición. Por ejemplo, si en una sala de presión negativa el paciente llevara una mascarilla quirúrgica durante un periodo de tiempo antes de la entrada de un trabajador sanitario, para varios intercambios de aire la exposición se reduciría considerablemente. Esta observación se aplica a todas las habitaciones, pero la magnitud del efecto depende de la interacción del control de la fuente con el entorno de la habitación, como se observa en la habitación de presión negativa.
Nuestros datos pueden ayudar a diseñar mejores mascarillas. En la habitación de hospital, al producirse un aumento de la fuga hacia el exterior en la Fuente (menos aerosol capturado por la mascarilla) había una protección reducida (FPR reducido) en el Receptor. Reducir la resistencia de la pieza bucal disminuiría la fuga hacia el exterior y podría compensar los defectos con el ajuste de la mascarilla.[Citation24]
Durante la tos, el control de la fuente fue claramente superior al uso de una mascarilla en el Receptor. En la cámara de presión negativa, la colocación de una mascarilla quirúrgica de ajuste natural (F-SMnat) en la Fuente durante la tos redujo la exposición en aproximadamente 1,500 veces (FPR = 1,587), en comparación con el extremo de sellar una mascarilla autofiltrante N95 (R-N95-vas) a la cara del receptor (FPR = 17). Esta observación se debió a los efectos combinados de la impactación de partículas expulsadas en la mascarilla () y la extracción de partículas desviadas por el flujo de aire en la habitación. Tales hallazgos fueron consistentes con los resultados reportados por Cheong y Phua,[Citation18] quienes encontraron que, en una sala de presión negativa, colocar el escape de ventilación en la pared ubicada detrás de la cama del paciente, como en nuestros experimentos, era más eficaz para eliminar contaminantes que un escape de ventilación ubicado en el techo, por encima del paciente.[Citation18]
Nuestro estudio tiene varias limitaciones. Las direcciones del flujo de aire y la posición de la cabeza fueron fijas, por lo que los cambios de dirección pueden afectar nuestras observaciones. Además, en un ambiente de hospital real el flujo de aire y la ventilación pueden variar en función del diseño de la habitación, la ubicación de las rejillas de ventilación y la posición del paciente y el personal sanitario. Nuestras posiciones de cabeza y el flujo de aire estaban en una dirección optimizada para la protección del personal de la salud, desde el Receptor hasta la Fuente. Esto puede aumentar el efecto reportado en el control de la Fuente. Sin embargo, los parámetros que hemos elegido para la ventilación y la magnitud y dirección del flujo de aire son típicos de los reportados para las habitaciones de hospital en estudios anteriores.[Citation25] Además, Lindsley et al. encontraron que la exposición a aerosoles potencialmente infecciosos en cualquier parte de la habitación no se veía afectada por la posición de la cabeza. [Citation25]
Nuestros aerosoles son acuosos, de modo que la distribución de partículas se verá afectada por cambios en la humedad relativa del ambiente. Aunque esta varió, los nebulizadores húmedos proporcionaron aire saturado, por lo que los aerosoles que salían del maniquí Fuente siempre eran poco sensibles a la humedad ambiental.
Si bien nuestro estudio no utilizó métodos formales de prueba de ajuste para llegar a valores de FPR seguros, empleamos un conjunto de mediciones para lograr un factor de ajuste equivalente (por ejemplo, una reducción de la exposición debida al uso de una mascarilla). Como se informó en nuestro estudio anterior, centrado en los efectos de pruebas de diferentes tipos de maniquíes en nuestra medición del ajuste, las pruebas de ajuste en maniquíes son complejas.[Citation21] En ese estudio reportamos que la mejora del ajuste fue cuantificada fácilmente por nuestras técnicas, permitiendo separar los efectos causados por los cambios en el control de la Fuente y los cambios en el ajuste en el Receptor. Muchos estudios con maniquíes simplemente sellan la mascarilla al maniquí para evitar este problema. Creemos que nuestros resultados relativos a mascarillas selladas y no selladas proporcionan una mayor comprensión de la interacción entre los factores implicados en las exposiciones reales, más allá de la mera protección del Receptor.
Nuestros datos ayudarán a diseñar futuros ensayos clínicos. En las pruebas de eficacia de la mascarilla quirúrgica/autofiltrante se debe incluir un brazo de control de la fuente.
Agradecimientos
Los autores agradecen a Lorraine Morra por su ayuda en la realización de los experimentos, así como en la creación del manuscrito y las figuras.
Referencias
- Nicas, M., R.M. Jones: Relative contributions of four exposure pathways to influenza infection risk. Risk Anal. Off. Publ. Soc. Risk Anal. 29:1292–1303 (2009). doi:https://doi.org/10.1111/j.1539-6924.2009.01253.x
- Centers for Control and Prevention of Diseases (CDC): Prevention Strategies for Seasonal Influenza in Healthcare Settings Guidelines and Recommendations. Disponible a través de http://www.cdc.gov/flu/professionals/infectioncontrol/healthcaresettings.htm2013.
- Siegel, J.D., E. Rhinehart, M. Jackson, L. Chiarello, y el Healthcare Infection Control Practices Advisory Committee: 2007 Guideline for Isolation Precautions: Preventing Transmission of Infectious Agents in Healthcare Settings (2007).
- Loeb, M., N. Dafoe, J. Mahony, et. al.: Surgical mask vs N95 respirator for preventing influenza among health care workers: a randomized trial. JAMA 302:1865–1871 (2009). doi:https://doi.org/10.1001/jama.2009.1466
- Berger, S.A., M. Kramer, H. Nagar, A. Finkelstein, A. Frimmerman, H.I. Miller: Effect of surgical mask position on bacterial contamination of the operative field. J. Hosp. Infect. 23:51–54 (1993). doi:https://doi.org/10.1016/0195-6701(93)90130-R
- Qian, Y., K. Willeke, S.A. Grinshpun, J. Donnelly, C.C. Coffey: Performance of N95 respirators: filtration efficiency for airborne microbial and inert particles. Am. Indust. Hyg. Assoc. J. 59:128–132 (1998). doi:https://doi.org/10.1080/15428119891010389
- Dispositivos de cirugía general y plástica: ódigo de Regulaciones Federales. Título 21. Administración de Alimentos y Drogas de los Estados Unidos (FDA) y Departamento de Salud y Servicios Humanos de los Estados Unidos (DHHS), 2000.
- Balazy, A., M. Toivola, A. Adhikari, S.K. Sivasubramani, T. Reponen, S.A. Grinshpun: Do N95 respirators provide 95% protection level against airborne viruses, and how adequate are surgical masks? Am. J. Infect. Control. 34:51–57 (2006). doi:https://doi.org/10.1016/j.ajic.2005.08.018
- Balazy, A., M. Toivola, T. Reponen, A. Podgorski, A. Zimmer, S.A. Grinshpun : Manikin-based performance evaluation of N95 filtering-facepiece respirators challenged with nanoparticles. Ann. Occup. Hyg. 50:259269 (2006).
- Shine, K.I., B. Rogers, y L.R. Goldfrank : Novel H1N1 influenza and respiratory protection for health care workers. N. Engl. J. Med. 361:1823–1825 (2009). doi:https://doi.org/10.1056/NEJMp0908437
- Janssen, L., H. Ettinger, S. Graham, R. Shaffer, y Z. Zhuang: The use of respirators to reduce inhalation of airborne biological agents. J. Occup. Environ. Hyg. 10:D97–D103 (2013). doi:https://doi.org/10.1080/15459624.2013.799964
- Loeb, M., A. McGeer, B. Henry et al.: SARS among critical care nurses, Toronto. Emerg. Infect. Dis. 10:251–255 (2004). doi:https://doi.org/10.3201/eid1002.030838
- Johnson, D.F., J.D. Druce, C. Birch, M.L. Grayson: A quantitative assessment of the efficacy of surgical and N95 masks to filter influenza virus in patients with acute influenza infection. Clin. Infect. Dis. 49:275–277 (2009). doi:https://doi.org/10.1086/600041
- Lee, S.A., S.A. Grinshpun, T. Reponen: Respiratory performance offered by N95 respirators and surgical masks: human subject evaluation with NaCl aerosol representing bacterial and viral particle size range. Ann. Occup. Hyg. 52:177–185 (2008). doi:https://doi.org/10.1093/annhyg/men005
- Diaz, K.T., G.C. Smaldone: Quantifying exposure risk: surgical masks and respirators. Am. J. Infect. Control. 38:501–508 (2010). doi:https://doi.org/10.1016/j.ajic.2010.06.002
- Luna, K.: Design of hospital isolation rooms. En Business Briefing: Hospital Engineering & Facilities Management, 2004.
- Sehulster, L.M., C.R.Y.W. Chinn, M.J. Arduino, et al.: Recommendations from CDC and the Healthcare Infection Control Practices Advisory Committee (HICPAC), 2004.
- Cheong, K.W.D., S.Y. Phua : Development of ventilation design strategy for effective removal of pollutant in the isolation room of a hospital. Build. Environ. 41: (2009).
- Nikander, K., J. Denyer, M. Everard, G.C. Smaldone : Validation of a new breathing simulator generating and measuring inhaled aerosol with adult breathing patterns. J. Aerosol Med. 13:139–146 (2000). doi:https://doi.org/10.1089/089426800418668
- Dennis, J.H., O. Nerbrink: New nebulizer technology. En Drug Delivery to the Lung, H. Bisgaard, C. O'Callaghan, G.C. Smaldone (ed.). Boca Raton, FL: CRC Press, 2001. págs. 326 a 328.
- Mansour, M.M., G.C. Smaldone : Respiratory source control versus receiver protection: impact of facemask fit. J. Aerosol Med. Pulm. Drug. Deliv. 26:131–137 (2013). doi:https://doi.org/10.1089/jamp.2012.0998
- Nicas, M., W.W. Nazaroff, A. Hubbard: Toward understanding the risk of secondary airborne infection: emission of respirable pathogens. J. Occup. Environ. Hyg. 2:143–154 (2005). doi:https://doi.org/10.1080/15459620590918466
- Xie, X., Y. Li, H. Sun, L. Liu: Exhaled droplets due to talking and coughing. J. Roy, Soc. 6(Suppl 6):S703–S14 (2009).
- Skaria, S.D., G.C. Smaldone : Respiratory source control using surgical masks with nanofiber media. Ann. Occup. Hyg. 58(6):771–781 (2014).
- Lindsley, W.G., W.P. King, R.E. Thewlis, et al.: Dispersion and exposure to a cough-generated aerosol in a simulated medical examination room. J. Occup. Environ. Hyg. 9:681–690 (2012). doi:https://doi.org/10.1080/15459624.2012.725986