Abstract
El objetivo de este trabajo fue la evaluación del potencial de la espectroscopía de reflectancia en el infrarrojo cercano (NIRS) para el análisis del contenido mineral en muestras liofilizadas de nabizas y grelos (Brassica rapa L. var. rapa). Se aplicó el método de mínimos cuadrados parciales modificados (MPLS) para desarrollar ecuaciones de calibración (n=298). Se evaluó la capacidad predictiva de las ecuaciones de calibración obtenidas mediante un lote de muestras (n=69) independientes del colectivo de calibración. Los coeficientes de determinación (r2ve) y errores de predicción (SEP) obtenidos en la validación externa para los distintos minerales fueron K=0,86(SEP=4,90); Ca=0,91(SEP=1,66); P=0,73(SEP=0,86); Mg=0,85(SEP=0,32); Na=0,87(SEP=0,21); Fe=0,90(SEP=60,48); Zn=0,80(SEP=5,83); Mn=0,81(SEP=5,72)y Cu=0,62(SEP=1,13). Las ecuaciones para Ca y Fe fueron las que mostraron mayor capacidad predictiva. Estos resultados demuestran el potencial del NIRS para el análisis rápido, no destructivo y preciso del contenido mineral en nabizas y grelos.
The objective of this study was to evaluate the potential and accuracy of near-infrared reflectance spectroscopy (NIRS) for predicting the mineral content in lyophilized samples of turnip greens and turnip tops (Brassica rapa L. var. rapa). Mathematical treatments of the spectra and modified partial least squares regression (MPLS) were used for developing calibrations equations (n = 298). An independent set of samples (n = 69) was used to evaluate and validate the performance of the calibrations equations. The coefficients of determination obtained in the external validation (r2ev) and error of prediction (SEP) for the different minerals were K = 0.86 (SEP = 4,90), Ca = 0.91 (SEP = 1,66), P = 0.73 (SEP = 0,86), Mg = 0.85 (SEP = 0,32), Na = 0.87 (SEP = 0,21), Fe = 0.90 (SEP = 60,48), Zn = 0.80 (SEP = 5,83), Mn = 0.81 (SEP = 5,72) and Cu = 0.62 (SEP = 1,13).The calibration equations obtained for Ca and Fe showed the highest predictive ability These results support the idea that NIRS technology is suitable for the fast, non-destructive, and accurate prediction of mineral content in turnip greens and turnip tops.
Introducción
Las especies pertenecientes a la familia de las Crucíferas están consideradas como uno de los primeros grupos de plantas domesticadas por el hombre, y desde entonces el hombre ha sido capaz, mediante selección, de modificar casi todas las partes de la planta (raíces, tallos, hojas, inflorescencias y semillas) con vistas a su uso alimentario (hortícola, oleaginosa, condimento, pienso), industrial (fabricación de plásticos, lubricantes, combustibles) y ambiental (fitorremediación, biofumigación). El consumo de las especies hortícolas de esta familia de plantas ha experimentado un fuerte aumento en los países industrializados en los últimos años, debido al descubrimiento de las propiedades saludables de una serie de compuestos exclusivos que contienen, los glucosinolatos, capaces de proteger frente a la aparición de determinados tipos de cánceres (Farnham, Wilson, Stephenson, & Fahey, Citation2004; Traka & Mithen, Citation2009, Villatoro, Font, et al., Citation2012).
Brassica rapa fue la primera especie de Brassica domesticada por el hombre hace miles de años, apareciendo ya citada en la literatura sánscrita con el nombre de Siddharta, lo que prueba la antigüedad de su cultivo (Prakash, Citation1961). Existen numerosas subespecies de B. rapa originadas en dos centros de origen independientes, uno en Europa para los tipos oleaginosos y otro en Asia que dio lugar a las formas hortícolas (Gómez & Prakash, Citation1999).
En el norte de España y Portugal los cultivos hortícolas de Brassica rapa tienen una gran tradición, distribución y consumo, tanto en fresco como envasado (De Haro, Del Río, Cartea, & Ordás, Citation2006). De la misma planta se cosechan los nabos, que son la raíz engrosada (hipocotilo), las nabizas, que son las hojas vegetativas, y los grelos que son los tallos junto con las hojas florales previos a la floración de la planta, formando parte de numerosos platos de la cocina tradicional (p. ej. ‘Lacón con grelos’). Estos alimentos, al igual que los procedentes de otras especies hortícolas de Brassica se caracterizan por su bajo contenido en grasa y proteína y su alto contenido en fibras, minerales y vitaminas. Comparados con otras hortalizas destacan por su elevado contenido en vitaminas A, C, E, B6, K, luteína, carotenoides y folatos (Jahangir, Kim, Choi, & Verpoorte, Citation2009; Rosa, Citation1999; USDA, Citation2015). También son particularmente ricas en minerales potasio, cobre, magnesio, manganeso, hierro, zinc y calcio (Kopsell, Kopsell, Lefsrud, & Curran-Celentano, Citation2005).
Los métodos tradicionales de análisis del contenido en minerales por vía húmeda, como por ejemplo la espectrometría de absorción atómica (AAS), la espectrometría de emisión atómica de plasma acoplado inductivamente (ICP-AES), o la espectrometría de masas de plasma acoplado inductivamente (ICP- MS) son caros, lentos, agresivos con el medio ambiente y necesitan mano de obra especializada para su aplicación. Como alternativa a estos métodos, desde los últimos 40 años se viene utilizando la espectroscopía por reflectancia en el infrarrojo cercano (NIRS) para el análisis de una gran diversidad de componentes de la calidad en los alimentos, así como de otras sustancias de interés para la industria farmacéutica (Chavez et al., Citation2015), química (Feng, Wu, & Zeng, Citation2015; Foster, Kakani, Ge, & Mosali, Citation2013), alimentaria, incluyendo frutas y verduras (Font, Del Río-Celestino, Cartea, & De Haro-Bailón, Citation2005; Guo, Ni, & Kokot, Citation2016; Martínez, Font, Gómez, Blanco, & Del Río, Citation2014; Schmitt, Garrigues, & De La Guardia, Citation2014) y agrícola (Cozzolino, Fassio, & Fernández, Citation2003; De Haro et al., Citation2006; Dimov, Suprianto, Hermann, & Möllers, Citation2012; Murray, Citation1986; Norris, Barnes, Moore, & Shenk, Citation1976; Shenk & Westerhaus., Citation1993; Van Maarschalkerweerd & Husted, Citation2015).
Aunque los minerales no poseen bandas de absorción en la región del infrarrojo pueden estar asociados a estructuras orgánicas en forma de óxidos, quelatos u otras moléculas que permitan poder ser estimados mediante ecuaciones de calibración desarrolladas para el NIRS, como se ha comprobado en trabajos publicados previamente en otras matrices vegetales (Cozzolino & Moron, Citation2004; García et al., Citation2012; González, Hernández, & González, Citation2007; Liao, Wu, Chen, Guo, & Shi, Citation2012; Martínez et al., Citation2014; Menesatti et al., Citation2010; Plans, Simó, Casañas, & Sabaté, Citation2012; Villatoro, Moreno, et al., Citation2012).
Teniendo en cuenta el creciente interés por este cultivo, y con vistas a su extensión a otras regiones de la Península Ibérica, desde los últimos años se están desarrollando programas de mejora genética que nos permitan obtener variedades de nabizas y grelos adaptadas a las condiciones edafoclimáticas mediterráneas y de alto valor nutracéutico, con especial énfasis en el estudio del contenido en minerales y glucosinolatos en sus partes consumibles.
El objetivo del presente trabajo fue estudiar las posibilidades del NIRS para el análisis rápido y preciso del contenido en potasio (K), calcio (Ca), fósforo (P), magnesio (Mg), sodio (Na), hierro (Fe), zinc (Zn), manganeso (Mn) y cobre (Cu) en muestras de nabizas y grelos.
Materiales y métodos
Material vegetal
Durante los años agrícolas 2010–2011, 2011–2012 y 2012–2013, un conjunto de 25 variedades de Brassica rapa L. var. rapa se cultivaron en la finca experimental del IAS de Córdoba, (37º51ʹ N, 4º48ʹW, España) en un diseño de bloques al azar con 3 repeticiones. El clima es típico mediterráneo con un precipitación media de 650 mm, y el suelo es profundo, franco-arenoso, clasificado como Typic Xerofluvent.
Las variedades de Brassica rapa L. var. rapa procedían del Banco de Germoplasma de Brassica de la Misión Biológica de Galicia (CSIC), en donde habían sido evaluadas por sus características agronómicas y su aptitud para producción de nabizas y grelos. Durante cada año agrícola, y en el momento óptimo para consumo, se tomaron muestras de nabizas (4 a 5 hojas por planta) y de grelos (3 a 4 tallos florales por planta) de las plantas seleccionadas para cada una de las variedades estudiadas. En total se cosecharon 373 muestras (228 de nabizas y 145 de grelos), de las cuales 135 se cosecharon en 2010–2011, 160 muestras procedían de la cosecha 2011–2012 y 78 muestras se cosecharon en 2012–2013. Todo el material vegetal se lavó a fondo con agua del grifo para eliminar la suciedad y el polvo de la superficie y se finalizó con un lavado en agua desionizada. A continuación se almacenaron a −80°C hasta el momento de su liofilización, que se realizó en un equipo Telstar® modelo Cryodos-50 (Telstar, Terrasa, Spain). Las muestras liofilizadas se molieron en un molino IKA-Labortechnik® modelo A10, durante 20 segundos y se almacenaron en desecador hasta el momento de ser analizadas por el método de referencia o por el equipo NIRS.
Análisis del contenido mineral por métodos de referencia
Los minerales analizados en las 373 muestras de nabizas y grelos fueron K, Ca, P, Mg, Na, Fe, Zn, Mn y Cu. La digestión de la muestra se realizó por vía húmeda con ácido nítrico y ácido perclórico (Isaac & Johnson, Citation1990). Los análisis de Ca, Mg, Fe, Mn, Zn y Cu se llevaron a cabo por espectrofotometría de absorción atómica y los de Na y K se hicieron por emisión atómica. El equipo utilizado fue un espectrofotómetro de absorción atómica Varian® modelo SpectrAA-50/55, con llama de aire-acetileno y lámparas de cátodo hueco de un solo elemento y corrección de fondo con lámpara de deuterio para el análisis de Mn. Para la determinación de Ca y Mg, se añadió cloruro de lantano a fin de evitar interferencias aniónicas. El análisis de P, como ácido molibdo-vanado-fosfórico, se hizo por colorimetría (Association of Official Analytical Chemists, Citation1991) en un espectrofotómetro UV-visible (Beckman® modelo DU640).
Desarrollo de ecuaciones NIRS
Se utilizó un espectrofotómetro de infrarrojo cercano modelo 6500 (Foss-NIRSystems®, Inc., Silver Spring, MD, EE.UU.) para llevar a cabo los registros de los espectros de las muestras en modo de reflectancia. Se registró un espectro por cada muestra. Las muestras se colocaron en una cápsula redonda de 3 cm de diámetro, compuesta de vidrio de cuarzo y aluminio anodizado para evitar interferencias en la absorción. De cada muestra se obtuvieron los espectros de reflectancia en el intervalo de longitudes de onda de 400 a 2500 nm, a intervalos de 2 nm. La recogida de los datos espectrales y el análisis quimiométrico de los mismos se llevó a cabo mediante el programa WinISI II v1,50 (Infrasoft International, Port Matilda, PA, USA).
La detección de anómalos espectrales se realizó mediante un análisis de componentes principales (PCA) aplicado a todo el conjunto de la población basado en el cálculo de la distancia de Mahalanobis (H) (Shenk & Westerhaus, Citation1991, Citation1996). Éste análisis además de ser una herramienta para la selección de muestras del colectivo de calibración, es una técnica de gran utilidad en el análisis para transformar los datos espectrales originales (valores de absorbancia) en nuevas variables (componentes principales) ortogonales, eliminando con ello la colinealidad (información redundante) (Martens & Naes, Citation1989). Se utilizó el algoritmo CENTER incluido en el programa WinISI II (versión 1.50 Infrasoft International, Port Matilda, PA, USA) para el cálculo de las distancias H entre los espectros de las distintas muestras respecto al espectro medio. De acuerdo con Shenk and Westerhaus (Citation1991), las muestras con un valor del estadístico H superior a 3 unidades se definieron como espectros atípicos y se eliminaron para el desarrollo de las ecuaciones. Se encontraron un total de 6 espectros con valores de H comprendidos entre 3,045 y 21,33 que fueron eliminados del conjunto de muestras utilizado en el trabajo. El número final de muestras seleccionadas fue de 367 que fueron divididas en dos grupos: el conjunto de calibración compuesto por 298 muestras y fue usado para el desarrollo de las diferentes ecuaciones de calibración, y el grupo de validación externa formado por 69 muestras (20% del total) y fue usado para evaluar la capacidad predictiva de cada una de las ecuaciones desarrolladas. La selección de las muestras del grupo de validación externa se realizó a partir del listado de muestras ordenadas en base a sus valores de H, eligiendo 1 de cada 5 muestras del listado ordenado (Shenk & Westerhaus, Citation1991). De esta manera, las muestras de validación externa seleccionadas representan todo el intervalo de variabilidad del conjunto de la población (Hruschka, Citation2001). Para el desarrollo de las ecuaciones de calibración se aplicó el método de regresión por mínimos cuadrados parciales modificados (MPLS), del que se ha mostrado su utilidad para la evaluación de los minerales, utilizando todo el intervalo espectral (400–2500 nm) (Cozzolino & Moron, Citation2004; Font, Del Río-Celestino, & De Haro-Bailón, Citation2006; González et al., Citation2007; Martínez et al., Citation2014; Ward, Nielsen, & Møller, Citation2011).
Se aplicó el procedimiento de corrección de espectros SNV+DT que proporciona el programa WinISI para eliminar la dispersión debida a los efectos causados por las diferencias en tamaño de partícula o la variación de longitud de camino entre la dispersión de las muestras y ajustar la línea base (Barnes, Dhanoa, & Lister, Citation1989). Los tratamientos matemáticos seleccionados aplicado a los espectros fueron (1, 4, 4, 1) y (2, 5, 5, 2), donde el primer número indica el orden de derivada (primera o segunda derivada del logaritmo de 1/R), el segundo número es la amplitud o distancia entre los segmentos a sustraer, el tercer número es la longitud del segmento a ser suavizado y el cuarto número indica un segundo suavizado (Shenk, Workman, & Westerhaus, Citation1992). Los estadísticos que definen las ecuaciones de calibración obtenidas son el coeficiente de determinación (R2) que muestra el porcentaje de la variabilidad existente en las concentraciones de minerales explicado por la ecuación de regresión, y el error estándar de la calibración (SEC) que es el error estándar de los residuales para el colectivo de calibración. Hay que destacar que el error estándar de la calibración solamente nos indica el ajuste de los valores de referencia a la línea de regresión, por lo que no puede considerarse un estadístico adecuado para evaluar la validez de la ecuación de calibración obtenida (Shenk & Westerhaus, Citation1996).
Validación de las ecuaciones
Para evaluar la capacidad predictiva de las ecuaciones de calibración se utilizaron dos modelos de validación que permiten establecen una comparación (mediante diferentes criterios estadísticos) entre el valor verdadero (valor obtenido por método de referencia) y el valor estimado (valor obtenido por NIRS). En primer lugar se realizó una validación cruzada, basada únicamente en los datos empleados en la etapa de calibración, para calcular el número óptimo de términos de la regresión. El algoritmo selecciona diferentes colectivos de calibración y validación dentro del total de la población considerada, realizando con cada selección una simulación del algoritmo de regresión (Martens & Naes, Citation1989; Shenk & Westerhaus, Citation1991). Finalmente el programa de cálculo seleccionó la ecuación que hace mínimo el error estándar de validación cruzada (SECV). Los estadísticos resultantes de la validación cruzada fueron el coeficiente de determinación de la validación cruzada (r2vc), el error estándar de la validación cruzada (SECV), que representa el error estándar de los residuales para el colectivo de validación cruzada, y el estadístico (RPD) (Williams & Sobering, Citation1996) que es la relación entre la desviación estándar y el error estándar de la validación cruzada (SD/SECV). El RPDvc es un estadístico que permite la evaluación del SECV en función de la desviación estándar de los datos de referencia para la población en estudio (Williams, Citation2001).
En segundo lugar se realizó una evaluación de las ecuaciones de calibración seleccionadas con muestras que no intervinieron en la calibración (colectivo de validación, n = 69 en nuestro trabajo), proceso que se denomina validación externa (Bagchi, Sharma, & Chattopadhyay, Citation2016; Font, Del Río, Fernández, & De Haro, Citation2003; Kim, Lee, Shin, & Shin, Citation2014; Lee, Hwang, Lee, & Choung, Citation2014; Martínez et al., Citation2014; Sánchez, Garrido-Varo, Guerrero, & Pérez-Marín, Citation2013; Shenk & Westerhaus, Citation1991). Las estadísticas de la validación externa incluyen el coeficiente de determinación de la validación (r2ve), el error estándar de predicción (SEP), el RPDve (que es la relación SD/SEP) y el RER (Williams & Sobering, Citation1996) que es la relación entre el intervalo de los datos de cada mineral y el error estándar de la predicción. Los estadísticos RPD y RER permiten la comparación del rendimiento del modelo a través de poblaciones con diferentes desviaciones estándar (Cozzolino & Moron, Citation2004).
Las mejores ecuaciones de calibración para cada mineral se seleccionaron considerando la combinación óptima de los siguientes estadísticos de la validación externa: altos valores de los coeficientes de determinación (r2ve) y altos valores de RPDve y de RER. Aquellas ecuaciones cuyo RPD es superior a 3 se consideran con excelente capacidad de predicción, las que tienen RPD entre 2 y 3 permiten realizar predicciones aproximadas, y aquellas cuyo RPD está entre 1,5 y 2 sólo pueden utilizarse con fines de clasificación en grupos de alto-medio-bajo contenido. Igualmente, los valores de RER obtenidos con las distintas ecuaciones de calibración con buena capacidad predictiva deben ser mayores de 10 (Williams & Sobering, Citation1996; Williams, Citation2001).
El error estándar de laboratorio (SEL) para el análisis de minerales se determinó y se comparó con el SEP para todas las ecuaciones. Se seleccionaron 10 muestras y se analizaron por duplicado en diferentes momentos y por diferentes analistas, para obtener una estimación del error total del método de referencia. La relación SEP/SEL también fue calculada, este estadístico permite relacionar el error de NIRS con el error en el método de referencia.
Resultados y discusión
Análisis de referencia de minerales en Brassica rapa
El contenido en minerales de las muestras de nabizas y grelos analizadas por el método de referencia (vía húmeda) se muestra en la . Estos resultados confirman que Brassica rapa es una buena fuente de minerales con concentraciones muy altas en K (valor medio de 34,27 g/kg), Ca (13,38 g/kg) y P (4,93 g/kg) y concentraciones más bajas de Na (1,18 g/kg), Mg (1,95 g/kg), Mn (33,15 mg/kg), Fe (269,19 mg/kg), Zn (39,2 mg/kg) y Cu (6.84 mg/kg). Estos valores superan a los encontrados en otras hortalizas como el calabacín (de 800 a5100 mg/kg en la pulpa y de 100 a 5900 mg/kg en la piel) (Martínez et al., Citation2014). El intervalo de contenido en K encontrado en las muestras de nabizas y grelos (de 13,39 a142,85 g/kg) también es alto y mayor que el encontrado en brócoli para este mineral (de 321,58 a 521,78 mg/100 g muestra fresca) (Dos Santos et al., Citation2013).
Tabla 1. Contenido en minerales de las muestras (n = 373) de Brassica rapa, analizadas según el método de referencia.
Table 1. Mineral content of Brassica rapa samples (n = 373) analysed by reference method.
Calibración y validación
Las muestras fueron divididas en el grupo de calibración (n = 298) y grupo de validación externa (n = 69). En la se muestran el intervalo, la media, la desviación estándar y el coeficiente de variación del contenido en minerales de las muestras pertenecientes a estos grupos. Los resultados de las ecuaciones de calibración obtenidas por regresión MPLS se muestran en la . Para el desarrollo de las ecuaciones NIRS de los minerales Na, Ca, P, Fe, Cu, Zn, se obtuvieron los mejores resultados aplicando la segunda derivada a los datos espectrales (2, 5, 5, 2; SNV + DT). En el caso de K, Mn y Mg los mejores resultados se obtuvieron tras aplicar la primera derivada a los datos espectrales (1, 4, 4, 1; SNV + DT). Todas las ecuaciones obtenidas presentaron unos valores altos en el coeficiente de determinación de la calibración, superiores a 0,9 para Ca (0,94), Fe (0,93), Na (0,93), K (0,92), Mg (0,9) y Mn (0,9), siendo inferiores para P (0,88), Zn (0,85) y Cu (0,72) (). Un coeficiente de determinación mayor de 0,9 indica que más del 90% de la varianza en los datos puede ser explicada por el modelo desarrollado, el 10% restante es atribuible a otros factores como la preparación de la muestra o los análisis de referencia (Williams, Citation2001). Los R2 obtenidos para cada uno de los minerales resultaron más altos que los obtenidos en otras verduras como Eruca vesicaria Na = 0,66, Cu = 0,52, Fe = 0,78, Mn = 0,41, K = 0,79, Ca = 0,39, Mg = 0,44 y Zn = 0,71 (Villatoro, Moreno, et al., Citation2012).
Tabla 2. Contenido en minerales del grupo de calibración y del grupo de validación externa de las muestras (n = 373) de Brassica rapa, analizadas según el método de referencia.
Table 2. Mineral content of calibration and validation sets of Brassica rapa samples (n = 373) analyzed by the reference method.
Tabla 3. Estadísticos de calibración y de validación cruzada para contenido en minerales en muestras de Brassica rapa utilizando SNVD+DT y primera o segunda derivadas.
Table 3. Calibration and cross-validation statistics for mineral content in samples of Brassica rapa using SNVD+DT and first or second derivatives.
Las ecuaciones de calibración finales para cada mineral fueron seleccionadas en base a maximizar el r2vc y a minimizar el SECV. Los valores de estos estadísticos obtenidos para las ecuaciones de calibración de los diferentes minerales fueron, de mayor a menor: Ca = 0,92 (SECV = 1,5); K = 0,9 (4,07); Na = 0,89 (0,19); Fe = 0,89 (57,56); Mg = 0,87 (0,29); Mn = 0,87 (4,43); P = 0,82 (0,7); Zn = 0,8 (5,69) y Cu = 0,66 (1,08). El intervalo de los valores del coeficiente de variación (CV) de la validación cruzada está comprendido entre 11,56% para el Ca y 28,79% para el Na; en la validación externa el intervalo del CV para los distintos minerales está comprendido entre el 12,57% para el Ca y el 31,34% para el Na. Estos valores son similares a los obtenidos por otros autores en calabacín, en donde el intervalo del CV de la validación cruzada está comprendido entre el 12,22% del Zn y 45,71% del Cu, y en la validación externa el intervalo del CV está comprendido entre 13,73% de Mg al 65,38% del Cu (Martínez et al., Citation2014). Los valores de RPDvc de la validación cruzada para cada mineral varían entre 3,47 para el Ca y 1,73 para el Cu (). En algunos casos (Ca, Mg), estos valores superan a los descritos en la bibliografía para los mismos minerales contenidos en otras matrices vegetales: en alfalfa Ca = 3,10 (González et al., Citation2007); en hojas de naranja Ca = 1,5 y Mg = 2 (Menesatti et al., Citation2010); en Eruca vesicaria Ca = 0,78 y Mg = 1,1 (Villatoro, Moreno, et al., Citation2012) y en tomate Ca = 2,73 y Mg = 2,51 (García et al., Citation2012); y en otros minerales los valores obtenidos en este trabajo también superan a otros descritos en cidra: K = 1,2, P = 1,4 y Fe = 1,7 (Liao et al., Citation2012). Merece la pena destacar el RPDvc obtenido para la ecuación de calibración del Ca (3,47) ya que está considerado un micronutriente esencial que, en el norte de España y Portugal, es aportado a la dieta fundamentalmente a través del consumo de plantas de Brassica como las nabizas y los grelos. Los valores de RPDvc superiores a 3 que se obtuvieron para Ca, K, Na y Fe son indicativos de que las ecuaciones de calibración pueden utilizarse con fines de diagnóstico e investigación. Las ecuaciones para el resto de los minerales, con una RPDvc inferior a 3, solamente permiten realizar una predicción aproximada del contenido en dichos minerales (Williams & Sobering, Citation1996). En la se representan los valores de laboratorio frente a los de predicción de NIRS para los minerales objeto de nuestro estudio en el grupo de muestras de la validación cruzada.
Figura 1. Representación gráfica de los valores de referencia frente a los valores de predicción en validación cruzada respecto al contenido en minerales de Brassica rapa.
Figure 1. Scatter plot of reference data vs. predicted values by NIRS of mineral content in Brassica rapa.
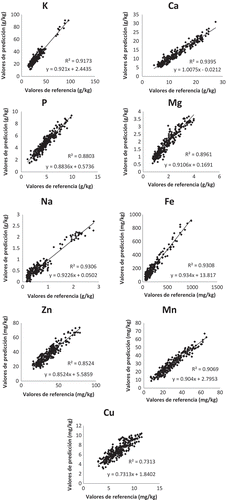
Una vez seleccionadas las ecuaciones de calibración para cada mineral, se procedió a su evaluación mediante el empleo de las mismas para la predicción del colectivo de validación, que contenía espectros de 69 muestras de nabizas y grelos, no incluidas en la calibración. En la , presentamos los estadísticos de la validación externa obtenidos para las ecuaciones de cada uno de los minerales estudiados. En general se obtuvieron elevados valores para los coeficientes de determinación de la predicción (r2ve) de las ecuaciones de la mayoría de los minerales: Ca (0,91), Fe (0,9), Na (0,87), K (0,86), Mg (0,85), Mn (0,81) y Zn (0,8), siendo los más bajos los del P (0,73) y del Cu (0,62). Los valores de RPDve más altos se obtuvieron para Fe (3,11), Ca (3,10), Na (2,71) y K (2,68), confirmando los resultados de RPDvc obtenidos en la validación cruzada, así como su utilidad para predecir el contenido de estos minerales en muestras independientes a las utilizadas en la calibración. Comparados con la bibliografía (Martínez et al., Citation2014; Plans, Simó, Casañas, & Sabaté, Citation2012) los valores de RPDve obtenidos en nuestro trabajo para los minerales K (2,68), Mg (2,50), Na (2,71), Fe (3,11), Mn (2,18), P (1,83), Ca (3,10), Zn (1,76) y Cu (1,35) son los más altos descritos hasta ahora, del mismo orden respecto al Ca, e inferiores a los valores descritos en otras matrices vegetales respecto al Zn y Cu.
Tabla 4. Estadísticos de la validación externa (n = 69) aplicados a las ecuaciones de calibración del contenido mineral de Brassica rapa.
Table 4. Statistics of external validation (n = 69) applied to the calibration equations of mineral content in Brassica rapa.
Se obtuvieron valores de RER superiores a 10 en los siguientes minerales: Ca (RER = 14,73), Fe (14,25), K (13,93), Na (RER = 11,76), Mg (RER = 10,22) y Mn (10,19), lo que es una prueba adicional de la elevada capacidad predictiva de los modelos de calibración desarrollados para estos minerales (Williams & Sobering, Citation1996; Williams, Citation2001).
Para evaluar la capacidad de precisión de las ecuaciones en relación al error del método de referencia se calculó el SEL para cada mineral y se relacionó con el SEP (SEP/SEL). En base a los valores de la relación SEP/SEL se puede decir que la precisión de las ecuaciones para los distintos minerales se puede clasificar como de excelente exactitud para K (SEP/SEL = 1,65), Ca (SEP/SEL = 1,48), Zn (SEP/SEL = 1,38) y Cu (SEP/SEL = 1,79); de buena exactitud para P (SEP/SEL = 3,58), Mg (SEP/SEL = 2,29), Fe (SEP/SEL = 2,71) y Mn (SEP/SEL = 2,36); y de baja exactitud para Na (SEP/SEL = 5,25) (Font et al., Citation2003). Los resultados obtenidos tanto en la validación cruzada como en la validación externa confirman la fiabilidad y capacidad de las ecuaciones de calibración desarrolladas para predecir de forma exacta y precisa el contenido en Ca y Fe en muestras de nabizas y grelos a partir de sus espectros de reflectancia en el infrarrojo cercano. Estas ecuaciones permiten utilizar la técnica NIRS para el análisis del contenido en Ca y Fe con fines de investigación, de control de calidad y cribado en Brassica rapa, lo que tiene especial importancia si se considera que los cultivos de esta especie son básicos en la dieta de las poblaciones del norte de España y Portugal, así como la importancia de estos minerales en la nutrición humana. Cabe señalar que las nabizas y los grelos tienen una alta concentración en calcio que es altamente biodisponible debido a estar asociado con bajos niveles de los ácidos oxálico y fítico (Lucarini, Canali, Cappelloni, Di Lullo, & Lombardi-Boccia, Citation1999).
En el caso de K, Na y Mg se obtuvieron valores de RPDve iguales o superiores a 2,5 y valores de RER superiores a 10, lo que las define como calibraciones aceptables para la predicción de estos minerales. El modelo desarrollado para el Mn obtuvo un valor de RPDve de 2,18 y de RER superior a 10, indicando que la ecuación de calibración solamente es utilizable para realizar predicciones cuantitativas aproximadas del contenido mineral. Los estadísticos obtenidos en la validación externa de las ecuaciones de P y Zn nos indican que solamente pueden ser utilizadas para asignar las muestras analizadas a grupos de alto, medio y bajo contenido para estos minerales. Finalmente, la ecuación obtenida para Cu no permite predecir de forma fiable el contenido de este mineral a partir de sus espectros NIRS, como ya había sido puesto en evidencia para este mismo mineral en trabajos previos de Cozzolino y Moron (Citation2004) y de Martínez et al. (Citation2014). Por lo tanto, sería necesario aumentar el colectivo de muestras de calibración con nuevas muestras que aumenten el intervalo de variabilidad respecto al contenido en este mineral, con vistas a seguir estudiando el potencial de la técnica NIRS para predecir este mineral.
Conclusiones
Se han desarrollado por primera vez ecuaciones de calibración que permiten la utilización de la espectroscopía de reflectancia en el infrarrojo cercano (NIRS) para el análisis rápido, simultáneo y preciso del contenido en Ca, Fe, K, Na y Mg en muestras de nabizas y grelos, al mismo tiempo que se puede obtener también una estimación aproximada del contenido en Mn, P y Zn.
Estos resultados demuestran la utilidad de la técnica NIRS como una herramienta fundamental tanto en los programas de mejora genética de la calidad de Brassica rapa L. var. rapa, (facilitando y abaratando las tareas de cribado, caracterización y selección de genotipos), como en los trabajos de control de la calidad nutritiva de los productos obtenidos.
Declaración de divulgación
No hay posible conflicto de intereses por los autores.
Agradecimientos
Agradecimiento al Ministerio de Economía y Competitividad del gobierno español por la financiación del proyecto: Genética y Mejora de Brasicas hortícolas: papel de los metabolitos secundarios. Referencia AGL2012-35539.
Referencias
- Association of Official Analytical Chemists. (1991). Official Methods 991.25. Second supplement. In K. Helrich (Eds.), Official methods of analysis (15th ed.). Arlington, VA: Author.
- Bagchi, T. B., Sharma, S., & Chattopadhyay, K. (2016). Development of NIRS models to predict protein and amylose content of brown rice and proximate compositions of rice bran. Food Chemistry, 191, 21–27. doi:10.1016/j.foodchem.2015.05.038
- Barnes, R. J., Dhanoa, M. S., & Lister, S. J. (1989). Standard Normal Variate Transformation and De-trending of Near-infrared Diffuse Reflectance Spectra. Applied Spectroscopy, 43, 772–777. doi:10.1366/0003702894202201
- Chavez, P.-F., Sacré, P.-Y., De Bleye, C., Netchacovitch, L., Mantanus, J., Motte, H. … Ziemons, E. (2015). Active content determination of pharmaceutical tablets using near infrared spectroscopy as process analytical technology tool. Talanta, TALD1501660. doi:10.1016/j.talanta.2015.08.018
- Cozzolino, D., Fassio, A., & Fernández, E. (2003). Uso de la Espectroscopía de Reflectancia en el Infrarrojo Cercano para el análisis de calidad de ensilaje de maíz. Agricultura Técnica, 63(4), 387–393. doi:10.4067/s0365-28072003000400007
- Cozzolino, D., & Moron, A. (2004). Exploring the use of Near Infrared Reflectance Spectroscopy (NIRS) to predict trace minerals in legumes. Animal Feed Science and Technology, 111, 161–173. doi:10.1016/j.anifeedsci.2003.08.001
- De Haro, A., Del Río, M., Cartea, E., & Ordás, A. (2006). Mejora de la calidad en especies de Brassica. In G. Llácer, M. J. Díez, J. M. Carrillo, & M. Badenes (Eds.), Mejora genética de la calidad (pp. 415–447). España: Editorial Universidad de Valencia.
- Dimov, Z., Suprianto, E., Hermann, F., & Möllers, C. (2012). Genetic variation for seed hull and fibre content in a collection of European winter oilseed rape material (Brassica napus L.) and development of NIRS calibrations. Plant Breeding, 131, 361–368. doi:10.1111/pbr.2012.131.issue-3
- Dos Santos, A. M. P., Lima, J. S., Anunciação, D. S., Souza, A. S., Dos Santos, D. C. M. B., & Matos, G. D. (2013). Determination and Evaluation Employing Multivariate Analysis of the Mineral Composition of Broccoli (Brassica oleracea L. var. Italica). Food Analytical Methods, 6, 745–752. doi:10.1007/s12161-012-9475-6
- Farnham, M. W., Wilson, P. E., Stephenson, K. K., & Fahey, J. W. (2004). Genetic and environmental effects on glucosinolate content and chemoprotective potency of broccoli. Plant Breeding, 123, 60–65. doi:10.1046/j.0179-9541.2003.00912.x
- Feng, F., Wu, Q., & Zeng, L. (2015). Rapid analysis of diesel fuel properties by Near Infrared Reflectance Spectra. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 149, 271–278. doi:10.1016/j.saa.2015.04.095
- Font, R., Del Río, M., Fernández, J. M., & De Haro, A. (2003). Acid Detergent Fiber Analysis in oilseed Brassicas by Near-infrared Spectroscopy. Journal of Agricultural and Food Chemistry, 51, 2917–2922.
- Font, R., Del Río-Celestino, M., Cartea, E., & De Haro-Bailón, A. (2005). Quantification of glucosinolates in leaves of leaf rape (Brassica napus ssp. pabularia) by near-infrared spectroscopy. Phytochemistry, 66(2), 175–185. doi:10.1016/j.phytochem.2004.11.011
- Font, R., Del Río-Celestino, M., & De Haro-Bailón, A. (2006). The use of near-infrared spectroscopy (NIRS) in the study of seed quality components in plant breeding programs. Industrial Crops and Products, 24, 307–313. doi:10.1016/j.indcrop.2006.06.012
- Foster, A. J., Kakani, V. G., Ge, J., & Mosali, J. (2013). Rapid assessment of bioenergy feedstock quality by near infrared reflectance spectroscopy. Agronomy Journal, 105(6), 1487–1497. doi:10.2134/agronj2013.0100
- García, S., Gálvez, L. N., Alonso, A., Agulló, E., Rubio, F., Ruiza, J. J., & Moral, R. (2012). Quality assessment of tomato landraces and virus-resistant breeding lines: Quick estimation by near infrared reflectance spectroscopy. Journal of the Science of Food and Agriculture, 92, 1178–1185. doi:10.1002/jsfa.4661
- Gómez, C., & Prakash, S. (1999). Origin and domestication. In C. Gómez-Campo (Ed.), Biology of Brassica coenospecies (pp. pp. 33-58). Amsterdam: Elsevier Science B.V.
- González, I., Hernández, J. M., & González, J. M. (2007). Use of NIRS technology with a remote reflectance fibre-optic probe for predicting mineral composition (Ca, K, P, Fe, Mn, Na, Zn), protein and moisture in alfalfa. Analytical and Bioanalytical Chemistry, 387, 2199–2205. doi:10.1007/s00216-006-1039-4
- Guo, Y., Ni, Y., & Kokot, S. (2016). Evaluation of chemical components and properties of the jujube fruit using near infrared spectroscopy and chemometrics. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy, 153, 79–86. doi:10.1016/j.saa.2015.08.006
- Hruschka, W. R. (2001). Data Analysiss Wavelength Selection Methods. In P. C. Williams & K. H. Norris (Eds.), Near infrared technology in the agricultural, food industries (pp. 35–55). St. Paul, MN: American Association of Cereal Chemist.
- Isaac, R. A., & Johnson, W. C. (1990). Collaborative study of wet and dry ashing techniques for the elemental analysis of plant tissue by atomic absorption spectrophotometry. Journal of AOAC International, 58 (3), 436–440.
- Jahangir, M., Kim, H. K., Choi, Y. H., & Verpoorte, R. (2009). Health-Affecting Compounds in Brassicaceae. Comprehensive Reviews in Food Science and Food Safety, 8(2), 31–43. doi:10.1111/j.1541-4337.2008.00065.x
- Kim, Y.-J., Lee, H. J., Shin, H.-S., & Shin, Y. (2014). Near-infrared Reflectance Spectroscopy as a Rapid and Non-destructive Analysis Tool for Curcuminoids in Turmeric. Phytochemical Analysis, 25, 445–452. doi:10.1002/pca.v25.5
- Kopsell, D. E., Kopsell, D. A., Lefsrud, M. G., & Curran-Celentano, J. (2005). Variability in elemental accumulations among leafy Brassica oleracea cultivars and selections. Journal of Plant Nutrition, 27(10), 1813–1826. doi:10.1081/PLN-200026431
- Lee, M.-S., Hwang, Y.-S., Lee, J., & Choung, M.-G. (2014). . The characterization of caffeine and nine individual catechins in the leaves of green tea (Camellia sinensis L.) by near-infrared reflectance spectroscopy. Food Chemistry, 158, 351–357. doi:10.1016/j.foodchem.2014.02.127
- Liao, H., Wu, J., Chen, W., Guo, W., & Shi, C. (2012). Rapid diagnosis of nutrient elements in fingered citron leaf using near infrared reflectance spectroscopy. Journal of Plant Nutrition, 35(11), 1725–1734. doi:10.1080/01904167.2012.698352
- Lucarini, M., Canali, R., Cappelloni, M., Di Lullo, G., & Lombardi-Boccia, G. (1999). In vitro calcium availability from Brassica vegetables (Brassica oleracea L.) and as consumed in composite dishes. Food Chemistry, 64, 519–523. doi:10.1016/S0308-8146(98)00159-9
- Martens, H., & Naes, T. (1989). Multivariate calibration. Chichester: John Wiley and Sons.
- Martínez, D., Font, R., Gómez, P., Blanco, T., & Del Río, M. (2014). Determining the mineral composition in Cucurbita pepo fruit using near infrared reflectance spectroscopy. Journal of the Science of Food and Agriculture, 94(15), 3171–3180. doi:10.1002/jsfa.6667
- Menesatti, P., Antonucci, F., Pallottino, F., Roccuzzo, G., Allegra, M., Stagno, F., & Intrigliolo, F. (2010). Estimation of plant nutritional status by Vis-NIR spectrophotometric analysis on orange leaves [Citrus sinensis (L) osbeck cv. tarocco]. Biosystems Engineering, 105, 448–454. doi:10.1016/j.biosystemseng.2010.01.003
- Murray, I. (1986). Near infrared analysis of forages. In W. Haresign & D. J. A. Cole (Eds.), Recent advances in animal nutrition. Studies in the agricultural and food sciences (pp. 141–156). London: Butterworths, Reading.
- Norris, K. H., Barnes, R. F., Moore, J. E., & Shenk, J. S. (1976). Predicting forage quality by infrared reflectance spectroscopy. Journal of Animal Science, 43, 889–897.
- Plans, M., Simó, J., Casañas, F., & Sabaté, J. (2012). Near-Infrared Spectroscopy Analysis of Seed Coats of Common Beans (Phaseolus vulgaris L.): A Potential Tool for Breeding and Quality Evaluation. Journal of Agricultural and Food Chemistry, 60, 706–712. doi:10.1021/jf204110k
- Prakash, O. (1961). Food and drinks in ancient India (pp. 165–168). Delhi: Munshi Ram Manohar Lal.
- Rosa, E. A. S. (1999). Chemical composition. In C. Gómez-Campo (Eds.), Biology of Brassica Coenoespecies (pp. 315–357). Amsterdam: Elsevier Science B.V.
- Sánchez, M.-T., Garrido-Varo, A., Guerrero, J.-E., & Pérez-Marín, D. (2013). NIRS technology for fast authentication of green asparagus grown under organic and conventional production systems. Postharvest Biology and Technology, 85, 116–123. doi:10.1016/j.postharvbio.2013.05.008
- Schmitt, S., Garrigues, S., & De La Guardia, M. (2014). . Determination of the mineral composition of foods by infrared spectroscopy: A review of a green alternative. Critical Reviews in Analytical Chemistry, 44(2), 186–197. doi:10.1080/10408347.2013.835695
- Shenk, J. S., & Westerhaus, M. O. (1991). Population definition, sample selection, and calibration procedures for Near Infrared Reflectance Spectroscopy. Crop Science, 31, 469–474. doi:10.2135/cropsci1991.0011183X003100020049x
- Shenk, J. S., & Westerhaus, M. O. (1996). Calibration the ISI way. In A. M. C. Davies & P. Williams (Eds.), Near infrared spectroscopy: The future waves (pp. pp. 198-202). Chichester: NIR Publications.
- Shenk, J. S., & Westerhaus., M. O. (1993). Analysis of agriculture and food products by near infrared reflectance spectroscopy. [Monograph]. p116. Port Matilda, PA: Infrasoft International.
- Shenk, J. S., Workman, J. J., Jr., & Westerhaus, M. O. (1992). Application of NIR spectroscopy to agricultural products. In D. A. Burns & E. W. Ciurczak (Eds.), Handbook of Near-Infrared Analysis (pp. 383–431). NewYork, NY: Dekker.
- Traka, M., & Mithen, R. (2009). Glucosinolates, isothiocyanates and human health. Phytochemistry Reviews, 8, 269–282. doi:10.1007/s11101-008-9103-7
- US Department of Agriculture, Agricultural Research Service, Nutrient Data Laboratory. (2015, May). USDA National Nutrient Database for Standard Reference, Release 27 (revised). Version Current. Retrieved from http://www.ars.usda.gov/ba/bhnrc/ndl
- Van Maarschalkerweerd, M., & Husted, S. (2015). Recent developments in fast spectroscopy for plant mineral analysis. Frontiers in Plant Science, 6, 169. doi:10.3389/fpls.2015.00169
- Villatoro, M., Font, R., Saha, S., Obregón, S., Anter, J., Muñoz, A. … Del Río, M. (2012). In vivo biological activity of rocket extracts (Eruca vesicaria subsp. sativa (Miller) Thell) and sulforaphane. Food and Chemical Toxicology, 50(5), 1384–1392. doi:10.1016/j.fct.2012.02.017
- Villatoro, M., Moreno, R., Muñoz, A., Cardeñosa, V., Amaro, M. Á., Font, R., & Del Río, M. (2012). Characterization and prediction by near-infrared reflectance of mineral composition of rocket (Eruca vesicaria subsp. sativa and Eruca vesicaria subsp. vesicaria). Journal of the Science of Food and Agriculture, 92(7), 1331–1340. doi:10.1002/jsfa.v92.7
- Ward, A., Nielsen, A. L., & Møller, H. (2011). Rapid Assessment of Mineral Concentration in Meadow Grasses by Near Infrared Reflectance Spectroscopy. Sensors, 11, 4830–4839. doi:10.3390/s110504830
- Williams, P. C. (2001). Implementation of Near-Infrared technology. In P. C. Williams & K. H. Norris (Eds.), Near infrared technology in the agricultural, food industries (pp. 145–169). St. Paul, MN: American Association of Cereal Chemist.
- Williams, P. C., & Sobering, D. C. (1996). How do we do it: A brief summary of the methods we use in developing near infrared calibrations. In A. M. C. Davies & P. C. Williams (Eds.), Near Infrared Spectroscopy: The Future Waves (pp. 185–188). Chichester: NIR Publications.
